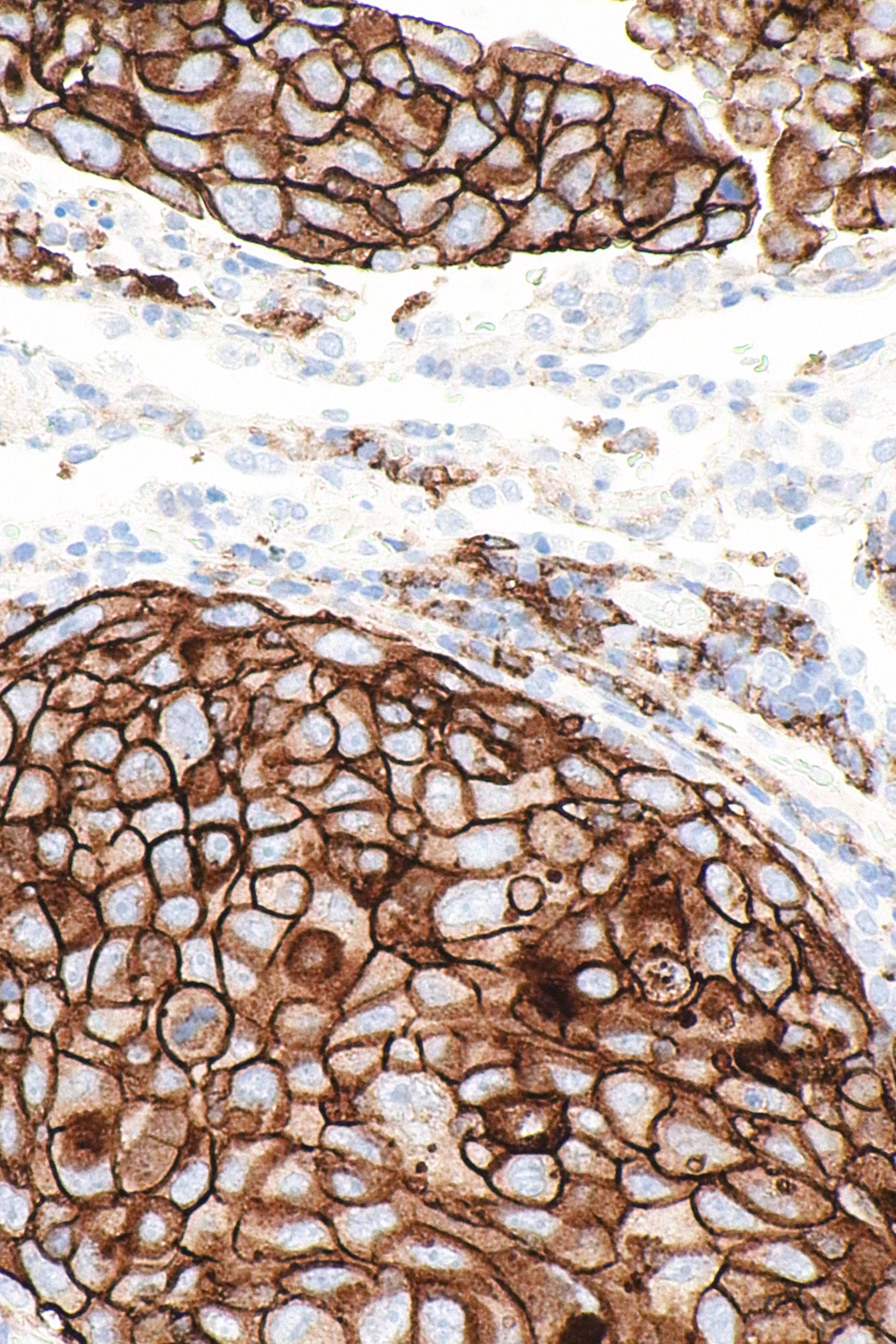
ما هي مثبطات PD-1 ومثبطات PD-L1؟
مثبطات PD-1 ومثبطات PD-L1 هي مجموعة من الأدوية المضادة للسرطان مثبطات نقاط التفتيش التي تمنع نشاط بروتينات نقطة التفتيش المناعية PD-1 و PDL1 الموجودة على سطح الخلايا. تظهر مثبطات نقاط التفتيش المناعية كعلاج أساسي لعدة أنواع من السرطان.
تعمل مثبطات PD-1 و PD-L1 على تثبيط ارتباط ليجند الموت المبرمج 1 (PD-L1) بمستقبلاته ، بروتين موت الخلية المبرمج 1 (PD-1). يشارك تفاعل بروتينات سطح الخلية هذه في قمع جهاز المناعة ويحدث بعد العدوى للحد من قتل الخلايا المضيفة المتفرجة ومنع أمراض المناعة الذاتية. هذا الحاجز المناعي نشط أيضًا أثناء الحمل ، بعد الطعم الخيفي للأنسجة ، وفي أنواع مختلفة من السرطان.
| اسم | استهداف | وافق |
|---|---|---|
| نيفولوماب | PD-1 | 2014 |
| بيمبروليزوماب | PD-1 | 2014 |
| أتيزوليزوماب | PD-L1 | 2016 |
| أفيلوماب | PD-L1 | 2017 |
| دورفالوماب | PD-L1 | 2017 |
| سيميبليماب | PD-1 | 2018 |
تاريخ
تم نشر مفهوم منع PD-1 و PD-L1 لعلاج السرطان لأول مرة في عام 2001. بدأت شركات الأدوية في محاولة تطوير عقاقير لمنع هذه الجزيئات ، وتم إطلاق أول تجربة إكلينيكية في عام 2006 لتقييم عقار نيفولوماب. اعتبارًا من عام 2017 ، تم إجراء أكثر من 500 تجربة سريرية تتضمن مثبطات PD-1 و PD-L1 في أكثر من 20000 مريض. بحلول نهاية عام 2017 ، تمت الموافقة على مثبطات PD-1 / PD-L1 لعلاج تسعة أشكال من السرطان.
العلاج المناعي للسرطان
في حالة المرض السرطاني ، يؤدي تفاعل PD-L1 على الخلايا السرطانية مع PD-1 على خلية T إلى تقليل إشارات وظيفة الخلايا التائية لمنع الجهاز المناعي من مهاجمة الخلايا السرطانية. يمكن أن يؤدي استخدام مثبط يمنع تفاعل PD-L1 مع مستقبلات PD-1 إلى منع السرطان من التهرب من جهاز المناعة بهذه الطريقة. يتم تجربة العديد من مثبطات PD-1 و PD-L1 داخل العيادة لاستخدامها في سرطان الجلد المتقدم ، وسرطان الرئة ذو الخلايا غير الصغيرة ، وسرطان الخلايا الكلوية ، وسرطان المثانة ، وسرطان الغدد الليمفاوية هودجكين ، من بين أنواع السرطان الأخرى.
يبدو أن العلاج المناعي باستخدام مثبطات نقطة التفتيش المناعية يقلص الأورام في عدد أكبر من المرضى عبر نطاق أوسع من أنواع الأورام ويرتبط بمستويات سمية أقل من العلاجات المناعية الأخرى ، مع استجابات دائمة. ومع ذلك ، فإن المقاومة المكتسبة و de-novo لا تزال تظهر في نسبة كبيرة من المرضى. ومن ثم تعتبر مثبطات PD-L1 فئة الأدوية الواعدة للعديد من أنواع السرطان المختلفة.
لا يستجيب جميع المرضى لمثبطات PD-1 / PD-L1. وافقت إدارة الغذاء والدواء على عدة فحوصات لقياس مستوى PD-L1 الذي تعبر عنه الخلايا السرطانية ، من أجل التنبؤ باحتمالية الاستجابة للمثبط. تم العثور على مستويات PD-L1 لتكون تنبؤية للغاية للاستجابة. عبء الطفرة الأعلى هو أيضًا تنبؤ بالاستجابة لعوامل مكافحة PD-1 / PD-L1.
ترتبط مثبطات PD-1 و PD-L1 ارتباطًا وثيقًا بمثبطات CTLA4 (البروتين 4 المرتبط بالخلايا اللمفاوية التائية السامة للخلايا) ، مثل إبيليموماب. يتم التعبير عن كل من PD-1 و CTLA-4 على الخلايا التائية المنشطة ، ولكن في مراحل مختلفة من الاستجابة المناعية.
تقوم التجارب السريرية الحالية بتقييم الأدوية المضادة لـ PD-1 و PD-L1 بالاشتراك مع أدوية العلاج المناعي الأخرى التي تمنع LAG3 و B7-H3 و KIR و OX40 و PARP و CD27 و ICOS.
المداواة
PD-1
بيمبروليزوماب (سابقًا MK-3475 أو lambrolizumab ، Keytruda) تم تطويره بواسطة Merck ، وتمت الموافقة عليه لأول مرة من قبل إدارة الغذاء والدواء في عام 2014 لعلاج سرطان الجلد. تمت الموافقة عليه لاحقًا لسرطان الرئة ذو الخلايا غير الصغيرة المنتشر وسرطان الخلايا الحرشفية في الرأس والرقبة. في عام 2017 ، أصبح أول دواء مناعي معتمد للاستخدام بناءً على الطفرات الجينية للورم بدلاً من موقع الورم. تبين أن المرضى الذين يعانون من عبء طفرة غير مترادفة أعلى في أورامهم يستجيبون بشكل أفضل للعلاج. تم إثبات أن معدل الاستجابة الموضوعية والبقاء على قيد الحياة بدون تقدم أعلى منه في المرضى الذين يعانون من انخفاض عبء الطفرة غير المترادفة.
نيفولوماب (Opdivo) تم تطويره بواسطة Bristol-Myers Squibb ، ووافقت عليه إدارة الغذاء والدواء لأول مرة في عام 2014 لعلاج سرطان الجلد. تمت الموافقة عليه لاحقًا لسرطان الرئة ذو الخلايا الحرشفية وسرطان الخلايا الكلوية وسرطان الغدد الليمفاوية هودجكين.
سيميبليماب تم تطوير (Libtayo) بواسطة Regeneron Pharmaceuticals ، وتمت الموافقة عليه لأول مرة من قبل FDA في عام 2018 لعلاج سرطان الخلايا الحرشفية الجلدي (CSCC) أو CSCC المتقدم محليًا الذين ليسوا مرشحين للجراحة العلاجية أو الإشعاع العلاجي.
تجريبي
حاليًا ، العديد من مثبطات PD-1 قيد التطوير:
- JTX-4014 من Jounce Therapeutics اعتبارًا من عام 2020 دخلت المرحلة الأولى من التجربة
- Spartalizumab (PDR001) هو مثبط PD-1 طورته شركة Novartis لعلاج كل من الأورام الصلبة والأورام اللمفاوية ، والتي دخلت اعتبارًا من 2018 المرحلة الثالثة من التجارب.
- Camrelizumab (SHR1210) هو جسم مضاد أحادي النسيلة مضاد لـ PD-1 قدمته شركة Jiangsu HengRui Medicine Co.، Ltd. التي حصلت مؤخرًا على موافقة مشروطة في الصين لعلاج ورم الغدد الليمفاوية هودجكين الكلاسيكي الانتكاس أو المقاوم للحرارة.
- Sintilimab (IBI308) ، جسم مضاد بشري مضاد لـ PD-1 تم تطويره بواسطة Innovent و Eli Lilly للمرضى المصابين بسرطان الرئة ذو الخلايا غير الصغيرة (NSCLC).
- Tislelizumab (BGB-A317) هو جسم مضاد أحادي النسيلة IgG4 مضاد لـ PD-1 في المرحلة المحورية 3 و 2 من التجارب السريرية في الأورام الصلبة والسرطانات الدموية.
- Toripalimab (JS 001) هو جسم مضاد أحادي النسيلة IgG4 متوافق مع البشر ضد PD-1 قيد الفحص السريري.
- Dostarlimab (TSR-042، WBP-285) هو جسم مضاد أحادي النسيلة متوافق مع البشر ضد PD-1 قيد التحقيق بواسطة GlaxoSmithKline
- INCMGA00012 (MGA012) هو جسم مضاد أحادي النسيلة IgG4 تم تطويره بواسطة Incyte و MacroGenics.
- AMP-224 من AstraZeneca / MedImmune و GlaxoSmithKline
- AMP-514 (MEDI0680) بواسطة AstraZeneca
PD-L1
أتيزوليزوماب (Tecentriq) هو جسم مضاد مؤنس بالكامل IgG1 (الغلوبولين المناعي 1) تم تطويره بواسطة شركة Roche Genentech. في عام 2016 ، وافقت إدارة الغذاء والدواء الأمريكية على عقار أتزوليزوماب لعلاج سرطان الظهارة البولية وسرطان الرئة ذو الخلايا غير الصغيرة.
أفيلوماب (Bavencio) هو جسم مضاد IgG1 بشري بالكامل تم تطويره بواسطة Merck Serono و Pfizer. أفيلوماب حاصل على موافقة إدارة الغذاء والدواء الأمريكية (FDA) لعلاج سرطان خلايا ميركل النقيلي. فشلت التجارب السريرية للمرحلة الثالثة لسرطان المعدة.
دورفالوماب (Imfinzi) هو جسم مضاد IgG1 بشري بالكامل تم تطويره بواسطة AstraZeneca. تمت الموافقة على Durvalumab من قِبل إدارة الأغذية والعقاقير (FDA) لعلاج سرطان الظهارة البولية وسرطان الرئة ذو الخلايا غير الصغيرة غير القابل للاكتشاف بعد العلاج الكيميائي.
تجريبي
يوجد ما لا يقل عن اثنين من مثبطات PD-L1 في المرحلة التجريبية من التطوير.
- KN035 هو الجسم المضاد الوحيد PD-L1 مع تركيبة تحت الجلد قيد التقييم السريري حاليًا في الولايات المتحدة والصين واليابان
- CK-301 بواسطة Checkpoint Therapeutics
- AUNP12 عبارة عن ببتيد 29 مير كأول مثبط هضمي PD-1 / PD-L1 تم تطويره بواسطة Aurigene و Laboratoires Pierre Fabre والذي يتم تقييمه في التجارب السريرية ، بعد في المختبر النتائج.
- CA-170 ، اكتشفه Aurigene / Curis باعتباره مضاد PD-L1 و VISTA ، تم اتهامه بأنه مثبط قوي للجزيء الصغير في المختبر. وبالتالي ، يخضع المركب حاليًا للمرحلة الأولى من التجارب السريرية على مرضى ورم الظهارة المتوسطة.
- BMS-986189 هو ببتيد حلقي كبير تم اكتشافه بواسطة Bristol-Myers Squibb ، حيث يتم حاليًا دراسة الحرائك الدوائية والسلامة والتحمل على موضوعات صحية.
الآثار السلبية
العلاجات المناعية كمجموعة لها تأثيرات غير مستهدفة وسميات مشتركة بينها. وتشمل بعض هذه الالتهاب الرئوي الخلالي ، والتهاب القولون ، والتهاب الكبد ، والتهاب الغدة الدرقية ، وردود فعل الجلد ، وانخفاض مستويات الصفائح الدموية وخلايا الدم البيضاء ، والتهاب الدماغ أو النخاع الشوكي ، والأحداث الضائرة العصبية العضلية بما في ذلك التهاب العضلات ، ومتلازمة غيلان باريه ، والوهن العضلي الشديد. التهاب عضلة القلب وقصور القلب ، قصور الغدة الكظرية الحاد والتهاب الكلية. التغييرات الأكثر شيوعًا المتعلقة بالكلى هي التهاب الكلية الخلالي الحاد ، تليها أمراض الكبيبات ثم التلف الأنبوبي. لم يتم توضيح الآلية التفصيلية لهذه الآثار الضارة بشكل كامل ؛ ومع ذلك ، فمن الواضح أنها تختلف عن أمراض المناعة الذاتية المعروفة. عادة ما تُعزى التفاعلات الضائرة المناعية إلى خلل معمم في الخلايا التائية أو تطوير الأجسام المضادة الذاتية ، على الرغم من أن استجابات خلايا الذاكرة التائية ضد الالتهابات الفيروسية الخفية قد تلعب أيضًا دورًا في بعض المرضى الذين يعانون من سرطان الجلد المتقدم بعد حصار PD-1 / CTLA-4 المشترك.
عند مقارنتها بعوامل العلاج الكيميائي القياسية ، كان لمثبطات PD-1 / PD-L1 معدل أقل للإصابة بالتعب ، والاعتلال العصبي الحسي ، والإسهال ، وكبت نخاع العظام ، وفقدان الشهية ، والغثيان ، والإمساك.
.







Discussion about this post